日本EGF協会認定原料および化粧品の活性測定試験
| 1.試験名 |
| 培養細胞を用いたEGFの活性測定 |
| 2.試験期間 |
| 2011年9月1日から2011年11月8日 |
| 3.試験目的 |
| 協会認定原料および化粧品についてEGF活性を測定し、認定基準要件を満たしているかどうかを調べる。 |
| 4.被験物質 |
| 次の2種類の被験物質を使用した。表1に示す。 |
表1.被験物質
| 被験物質番号 |
1 |
2 |
| 本報告書における被験物質名 |
協会認定EGF原料 |
協会認定化粧品 |
| 品名 |
ヒトオリゴペプチド-1 |
EGFエクストラエッセンス |
| ロット番号またはBatch No. |
20110301(2011年3月製造) |
KH1 (2011年8月製造) |
性状 |
白色の凍結乾燥粉末 |
無色透明の液体 |
公称EGF濃度 |
― |
0.167μg/mL |
公称活性 |
1.13x106IU/ |
167IU/mL |
容量 |
1mg入り |
60mL入り |
試験開始までの保存方法 |
冷蔵庫保存 |
常温保存 |
| 5.陽性対照物質 |
| The
National Institute for Biological Standards and Control(以下、NIBSC)から入手した標準EGFを 陽性対照物質として使用した。表2に示す。 |
表2.陽性対照物質
| 本報告書における 陽性対照物質名 |
標準EGF |
| 品名 |
EPIDERMAL GROWTH
FACTOR (EGF) Human, rDNA-derived |
| 販売元および品番 |
NIBSC code:
91/530 |
| ロット番号 |
― |
性状 |
凍結乾燥物 |
活性 |
2000IU/アンプル |
活性測定に使用した細胞 |
Balb/c
3T3 |
容量 |
2μg/アンプル |
| 比活性 |
1.00×106IU/mg EGF |
貯法 |
-40℃以下の保存を推奨 |
保存方法 |
溶解後は-80℃に設定した冷凍庫内で保存 |
| 6.細胞 |
| (独)理化学研究所、バイオリソースセンター細胞材料開発室(RIKEN Cell Bank)から入手した BALB/3T3 clone A31を使用した。表3に示す。 |
表3.細胞
表4.活性測定条件の概要
| 細胞名 |
BALB/3T3 clone
A31 |
| 本報告書における細胞名 |
A31 |
| 由来 |
マウス胎児(BALB/c) |
| ロット番号 |
013 |
購入時継代数 |
不明 |
細胞数、本数 |
1.3×106個/バイアル、1本 |
| 7.活性測定条件 |
| 測定対象 |
EGF |
| 測定時の培地 |
0.5%FBS、ゲンタマイシン10μg/mLを含むMEM |
| 細胞播種密度 |
2x103個/well、96well
plate |
| 培養条件 |
37℃、5%CO2 |
|
培養日数 |
播種後1日に被験物質または陽性対照物質を含む 上記培地に 交換し、5日間 |
|
細胞数の測定法 |
PicoGreen
® dsDNA Reagent(インビトロジェン社)に よるDNAの定量 |
| 8.試験方法 |
|
8-1.試験物質の調製 |
1mg/mLウシ血清アルブミン含有PBSで溶解した後、使用時まで-80℃で保存した。 |
|
8-2.EGFの活性測定 |
| 10%FBS、10μg/mLゲンタマイシンを含むMEMを用いて、37℃、5%CO2条件下で培養し、安定的に増殖させたA31を 試験に使用した。 A31細胞を96wellプレートに2x103個/well、5%FBS含有培地で播種して培養した。培養後24時間に、 0.5%FBS含有培地にて段階的に希釈した試験物質を含む培地に交換して、さらに5日間培養した。 試験物質を公比1.5あるいは2.25で段階希釈し、各濃度あたり3wellを使用した。EGF活性は、粉末試料について はED50(ng/mL)および国際単位による比活性(IU/mg EGF)として、溶液試料についてはED50(nL/mL) および国際単位濃度(IU/mL)として表記した。EGF濃度既知の溶液試料については、国際単位による 比活性(IU/mg EGF)も算出した。 細胞を1%NP-40含有緩衝液にて溶解した後、ウシ胸腺DNAを標準としてPicoGreen ® dsDNA Reagentを用いて測定した。 3wellの結果の平均値を算出し増殖曲線を作成した。 DNA量はwell当たりのDNA量として表記した。また、EGFの濃度を横軸、EGF非添加(ブランク)のDNA量を0、 最も高いDNA量を1としたDNA ratioを縦軸とした 増殖曲線を作成し、ED50の値を算出した。 |
| 9.結果 |
| 9-1-1.陽性対照物質(標準EGF)測定結果 |
| 試験は2回実施(試験1、試験2)した。増殖曲線を図1及び2に示す。標準EGFは、0.585ng/mL~4.44ng/mLあるいは 6.67ng/mLの間において、濃度依存的な増殖促進作用を示した。また、得られた結果に基づいて、ED50の算出用に 使用した回帰曲線の結果を図3及び4に示す。試験1のED50は1.06ng/mL、試験2のED50は0.816ng/mL、 平均値は0.938ng/mLであった。 |
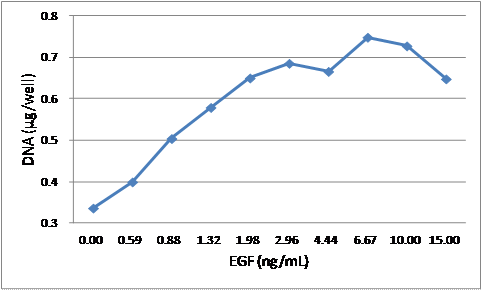 |
| 図1.A31に対する標準EGFによる増殖曲線(試験1)
縦軸は細胞数の指標であるDNA量、横軸はEGF濃度を示す。 |
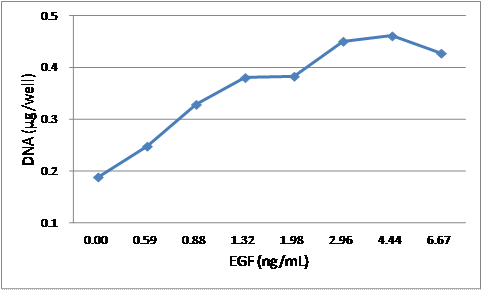 |
| 図2.A31に対する標準EGFによる増殖曲線(試験2) 縦軸は細胞数の指標であるDNA量、横軸はEGF濃度を示す。 |
 |
|
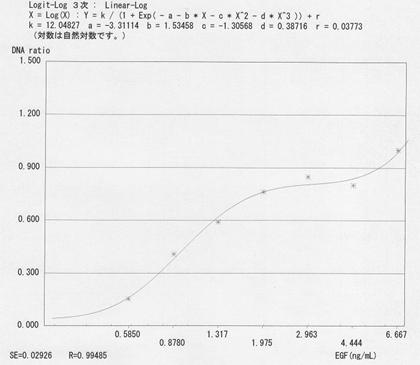
図3.A31に対する標準EGFによる増殖促進のED50(試験1) ED50付近の結果7点に基づいて、3次元多項式を用いて算出したED50は1.06ng/mLであった。 図中の式は3次元多項式、Rは相関係数を示す。 |
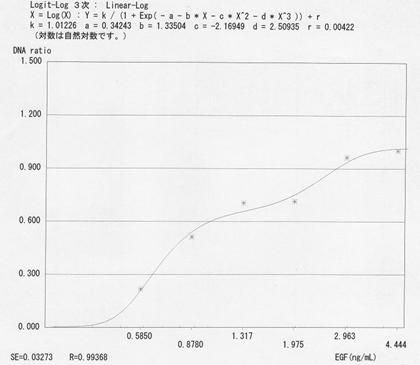 |
図4.A31に対する標準EGFによる増殖促進のED50(試験2) |
ED50付近の結果6点に基づいて、3次元多項式を用いて算出したED50は0.816ng/mLであった。 図中の式は3次元多項式、Rは相関係数を示す。 |
| 9-1-2標準EGFのまとめ |
| 表5に示す。標準EGFのED50を(独)理化学研究所から入手したBALB/3T3 A31を用いて測定した結果、 0.938ng/mLと算出された。ED50の値から算出された比活性は1.07×106IU/mg EGFで、 添付文書に記載されている値から算出した比活性である1.00×106IU/mg EGFと同様であった。 |
| 表5.標準EGFのまとめ |
|||
資料 |
使用細胞 |
ED50 |
比活性 |
|
標準EGFの 添付文書 |
Balb/c 3T3 |
1.00ng/mL (比活性からの換算値) |
1.00×106IU/mg EGF |
|
本試験報告書 |
BALB/3T3
A31((独)理化学研究所) |
1回目:1.06ng/mL 2回目:0.816ng/mL 平均:0.938ng/mL |
1.07×106IU/mg EGF |
| 9-2-1.協会認定EGF原料測定結果 |
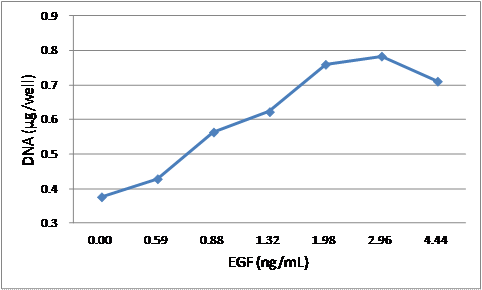
| 試験は2回実施(試験1、試験2)した。結果を図5及び6に示す。試験1及び試験2ともに、 協会認定EGF原料は0.585ng/mLから2.96ng/mLの間で濃度依存的な増殖促進作用を示した。 ED50の算出用に使用した回帰曲線の結果を図7及び8に示す。 試験1のED50は0.988ng/mL、 試験2のED50は0.996ng/mL、平均は0.992ng/mLであった。 |
 |
|
図5.A31に対する協会認定EGF原料による増殖曲線(試験1)
縦軸は細胞数の指標であるDNA量、横軸はEGF濃度を示す。 |
 |
|
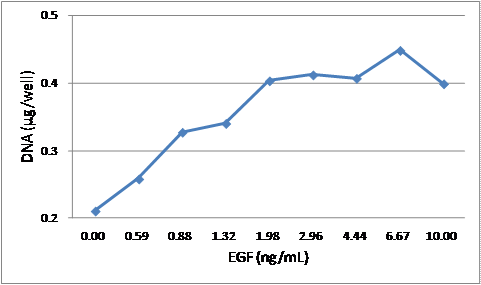
図6.A31に対する協会認定EGF原料による増殖曲線(試験2) 縦軸は細胞数の指標であるDNA量、横軸はEGF濃度を示す。 |
 |
|
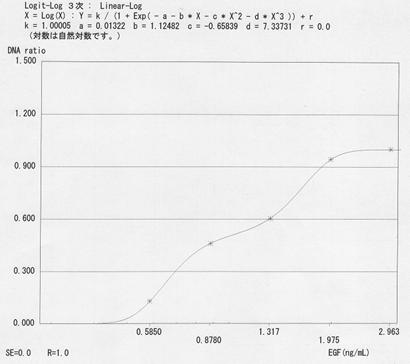
図7.A31に対する協会認定EGF原料による増殖促進のED50(試験1)
ED50付近の結果5点に基づいて、3次元多項式を用いて算出したED50は0.988ng/mLであった。 図中の式は3次元多項式、Rは相関係数を示す。 |
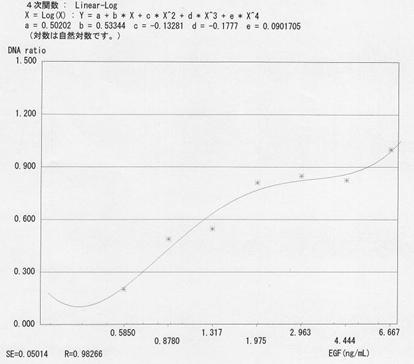 |
図8.A31に対する協会認定EGF原料による増殖促進のED50(試験2) ED50付近の結果7点に基づいて、4次元多項式を用いて算出したED50は0.996ng/mLであった。 図中の式は4次元多項式、Rは相関係数を示す。 |
| 9-2-2.協会認定EGF原料のまとめ |
| 表6に示す。協会認定EGF原料について、BALB/ 3T3
A31に対するED50を測定した結果、 0.992ng/mLと算出された。ED50の値から算出された比活性は1.01×106IU/mg EGFで、 CoAに記載されている比活性である1.13×106IU/mg EGFと同程度であった。 |
| 表6.協会認定EGF原料のまとめ |
|||
資料 |
使用細胞 |
ED50 |
比活性 |
| 協会認定EGF原料 (Lot.:20110301)のCoA |
記載なし |
0.885ng/mL (比活性からの換算値) |
1.13×106IU/mg EGF |
| 本試験報告書 |
BALB/3T3
A31((独)理化学研究所) |
1回目:0.988ng/mL 2回目:0.996ng/mL 平均:0.992ng/mL |
1.01×106IU/mg EGF |
| 9-3-1.協会認定化粧品(EGFエクストラエッセンス)測定結果 |
| エクストラエッセンスは、溶液試料として供給された。試験は2回実施(試験1、試験2)し、結果を図21及び22に示す。 試験1及び試験2ともに1.95μL/mL~22.2μL/mLの間で濃度依存的な増殖促進作用が認められた。 また、得られた結果に基づいて、ED50の算出用に使用した回帰曲線の結果を図23及び24に示す。 試験1のED50は5.55μL/mL(5550nL/mL)、試験2のED50は6.24μL/mL(6240nL/mL)、 平均値は5.90μL/mL(5900nL/mL)であった。 |
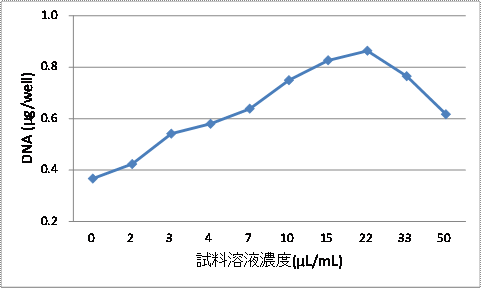 |
| 図21.A31に対するエクストラエッセンスによる増殖曲線(試験1) 縦軸は細胞数の指標であるDNA量、横軸は試料溶液濃度を示す。 |
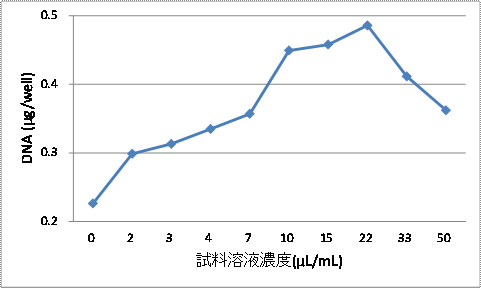 |
| 図22.A31に対するエクストラエッセンスによる増殖曲線(試験2) 縦軸は細胞数の指標であるDNA量、横軸は試料溶液濃度を示す。 |
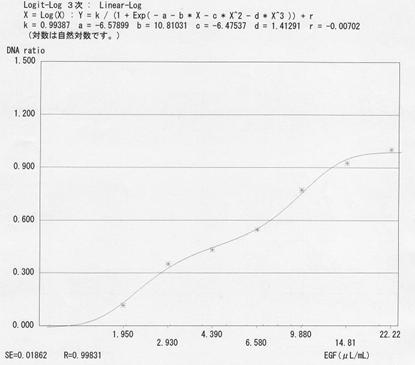 |
| 図中の式は3次元多項式、Rは相関係数を示す。 |
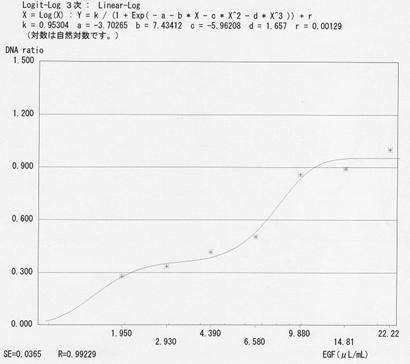 |
図24.A31に対するエクストラエッセンスによる増殖促進のED50(試験2) |
| |
| 表7に示す。エクストラエッセンスのED50について、A31を用いて測定した結果、 5.90μL/mL(5900nL/mL)と算出された。ED50から算出された国際単位濃度は169IU/mLであった。 比活性は1.01×106IU/mg EGFと算出された。 |
| 表7.エクストラエッセンスのまとめ |
||||
資料 |
使用細胞 |
ED50 |
国際単位濃度 |
比活性 |
| エクストラエッセンスの 公称 |
記載なし |
記載なし |
10,000IU/60mL |
記載なし |
|
本試験報告書 |
BALB/3T3
A31((独)理化学研究所) |
1回目:5550nL/mL |
169IU/mL(10,140IU/60mL) |
1.01×106
IU/mg EGF |
| 10.考察 |
| 本試験において測定された標準EGFのED50は0.938ng/mLで、この値から算出される比活性は1.07×106IU/mg EGFであった。 この値は標準EGFの添付文書に記載されている値から算出される比活性である1.00×106IU/mg EGFとほぼ同じであった。 以上の結果は、本試験で測定されたEGFのED50値を補正することなく、そのまま国際単位に変換できることを示している。 CoA記載の比活性である1.13×106IU/mg EGFと大きな差がなかった。 劣化はみられなかった。 協会認定化粧品(EGFエクストラエッセンス)の国際単位濃度は169IU/mLで、 1商品あたり10,140IU/60mLの活性を有することが判明した。 協会認定原料と同様な比活性のEGFを0.167μg/mLの濃度で 配合した被験物質であることが確認された。 |
| 11.文献 |
| 1.Instructions
for use: WHO International Standard, EPIDERMAL GROWTH FACTOR (EGF) Human, rDNA-derived, NIBSC code: 91/530, |
|
以上 |
| ホームに戻る |